糖类物质的过度摄入偏好是推动糖尿病发病率上升的重要因素。这种饮食倾向的形成涉及复杂的肠-脑信号传导机制,其中肠道微生物群落可能扮演关键调控角色。2025年1月,江南大学陈永泉与朱升龙课题组在《Nature Microbiology》(IF:20.5)发表重要研究成果:Free fatty acid receptor 4 modulates dietary sugar preference via the gut microbiota,阐明了游离脂肪酸受体4(Ffar4)通过肠道菌群调控糖类偏好的分子机制。
研究表明,Ffar4表达下调与高糖饮食行为相关,其缺失会导致肠道普通拟杆菌(Bacteroides vulgatus)丰度降低及代谢产物泛酸盐减少。泛酸盐通过促进GLP-1分泌,激活肝脏FGF21释放,进而作用于下丘脑神经环路,抑制糖类摄入欲望并调节能量代谢平衡。该发现揭示了全新的肠-肝-脑轴调控网络,为代谢性疾病的干预提供了潜在治疗靶点。

图1:论文题图
研究通过检测18只糖尿病模型小鼠和60例2型糖尿病患者的血液样本,并与24例健康人群对照比较,发现实验组的Ffar4的mRNA表达量明显下降。进一步在三种不同糖尿病动物模型中也证实,小鼠体内的Ffar4基因表达水平呈现显著下调趋势。这一结果表明Ffar4的表达异常可能与糖尿病发病机制存在关联。
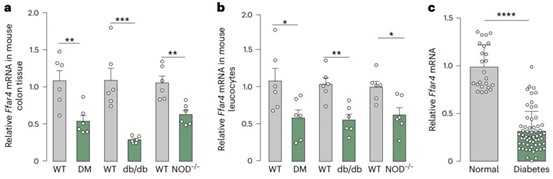
图2:糖尿病患者和糖尿病小鼠Ffar4表达水平显著降低
研究者对一个全基因组关联研究(GWAS)数据库进行了孟德尔分析,研究人员发现携带Ffar4基因突变的个体表现出对含糖食物(如甜味巧克力和加糖茶饮)的显著偏好。为验证这一现象,研究者构建了Ffar4基因敲除小鼠模型,观察到该品系小鼠同样出现糖类摄入量增加的行为特征。鉴于Ffar4主要在肠道组织中表达,且已有研究表明肠道微生物可调控宿主的饮食选择,研究者推测Ffar4可能通过影响肠道菌群来调节糖偏好。实验数据显示,Ffar4表达下调会导致肠道内普通拟杆菌(Bacteroides vulgatus)及其代谢产物泛酸盐的含量减少。相反,Ffar4过表达则能促进该菌群的增殖。机制研究表明,普通拟杆菌产生的泛酸盐能够有效刺激肠道L细胞分泌GLP-1,这可能是影响宿主糖代谢调控的关键途径。
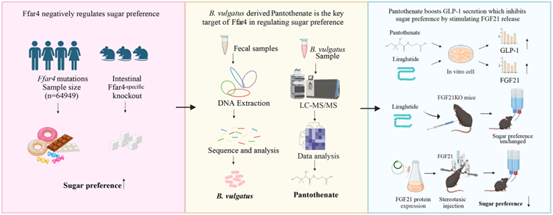
图3:机制图
泛酸盐负责GLP-1的分泌以及后续FGF21的分泌,GLP-1进一步调控了肝脏FGF21释放,FGF21则通过腹内侧下丘脑(VMH)抑制了糖偏好。接下来,研究团队证实,向糖尿病小鼠喂食泛酸盐,或在糖尿病小鼠中移植普通拟杆菌,均能显著减少它们寻求糖的行为,从而验证了这种复杂的肠-肝-脑信号轴。研究者猜测,Ffar4缺乏导致的糖偏好可能是糖尿病发展的重要因素,针对Ffar4或普通拟杆菌进行调控可能是预防糖尿病的快捷通道。最后,研究团队表示,需开展进一步临床研究分析,以验证这种肠-肝-脑信号轴是否能够作为控制肥胖以及糖尿病等代谢疾病的治疗靶点。
论文链接:https://www.nature.com/articles/s41564-024-01902-8











