近日,我校胥传来教授团队在手性等离子体和生命体系相互作用机制研究取得了重要进展,相关工作相继发表在Nature Communications, 2017, 8:1847 (https://www.nature.com/articles/s41467-017-01337-2.pdf); Nature Communications, 2017, 8: 2007 (https://www.nature.com/articles/ s41467-017-02268-8.pdf)上。
人工手性组装体与生物体系的相互作用,近年来引起广泛关注。胥传来教授研究团队将人工手性组装结构与细胞共孵育,系统研究了人工手性界面与生物界面的作用方式,首次发现了手性二聚体结构在细胞内的信号反转。研究表明,细胞内高盐浓度、高蛋白浓度改变了纳米粒子之间的静电斥力,进而引起了粒子间链接分子核酸的自发扭转。该研究为生物体系药物输运效率计算、纳米尺度相互作用定量分析提供了有效工具。同时,该团队研制了二维手性等离子膜,发现L手性膜可特异性地促进神经细胞的增殖和分化。进一步研究表明,L手性膜上细胞纤连蛋白表达水平显著高于D-手性膜和非手性膜;纤连蛋白的高表达,显著增强了神经细胞在基底上的粘附,进而促进了神经细胞的增殖和分化。
手性是自然界的普遍现象,与生命现象、药物设计合成以及光电材料开发等密切相关。上述研究成果为系统了解生命体系的信号传递、能量转移和交互过程提供了重要途径。博士后孙茂忠,博士生赵雪利分别为两篇论文的第一作者,青年教师徐丽广教授为两篇论文的共同第一作者,匡华教授为通讯作者。研究工作得到了国家自然基金重点项目(21631005),国家重点研发计划项目(2017YFA0206902)等项目的支持。
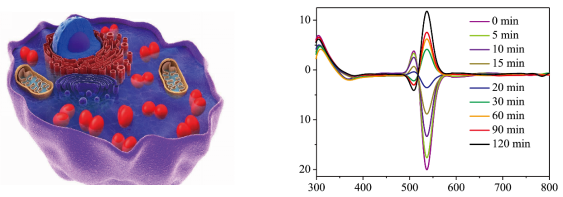
图1:细胞内等离子纳米二聚体组装结构的手性反转;
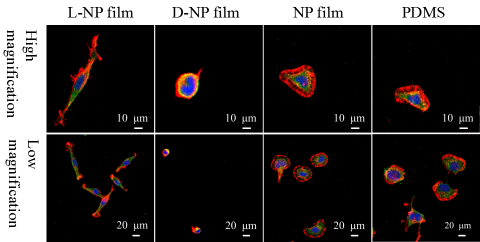
图2:神经细胞在手性金膜上的差异性增殖和分化;

















